Nanosurf Flex-FPM流体力学探针显微镜
纳米操作和单细胞生物学的成熟微流控工具
FluidFM探针显微镜 (FPM)将AFM的力灵敏度和位置精度与Cytosurge公司的FluidFM技术相结合,在单细胞生物学和纳米科学中实现了一系列激动人心的应用。
Nanosurf拥有为AFM系统提供附加FluidFM®的最长经验,是Cytosurge公司在这一创新技术方面的第一个合作伙伴——带FluidFM®系统的FlexAFM于2013年推出。附加FluidFM装置可用于FlexAFM和CoreAFM平台,以及FlexAFM上的独特的集成FPM的方案。


通过光学样品访问进行高度精确的压力、作用力和位置控制
完全集成的系统,配有界面友好的 FluidFM® ARYA 操作员软件
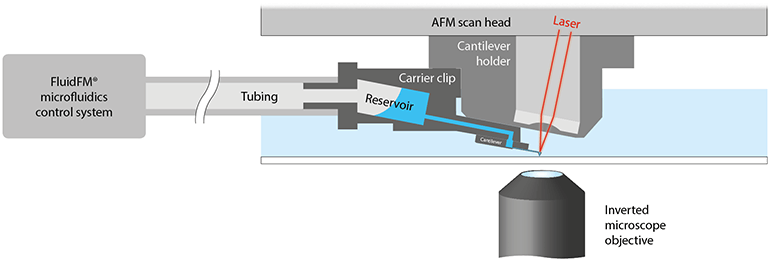
FluidFM®微流体控制系统
兼容于主要的倒置显微镜品牌
不同的FluidFM®探针: 专为特定应用而设计的空心悬臂
FluidFM® 微量移液管: 悬臂无针尖,带有末端开口
FluidFM® 纳米管: 悬臂带有最尖端开口
FluidFM® 快速成型探头: 带有封闭锥形尖端的悬臂,可用于FIB铣削
开拓性研究, 触手可及
在科学前沿进行原创性研究的工具
Flex-FPM开启了引人入胜的创新实验之门
 单细胞粘附
单细胞粘附
 胶质力谱
胶质力谱
 单细胞注射
单细胞注射
 点识别
点识别
 单细菌粘附
单细菌粘附
 单细胞隔离
单细胞隔离
 单细胞提取
单细胞提取
 纳米光刻
纳米光刻
结合光学、力学与流体控制的一体化方案
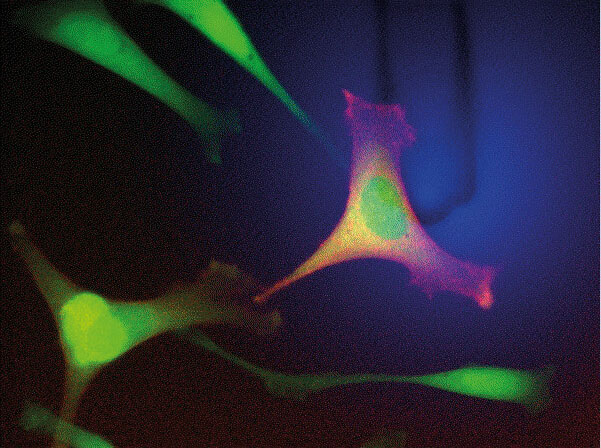

通过荧光属性来进行光学的细胞筛选(左图). 在力的控制下,将悬臂梁轻轻放置在细胞上,用一种共沉积荧光染料(蓝色)监测胰蛋白酶的施用。释放后,用相同的悬臂拾取该细胞,并将其与其余部分隔离,将其置于单独的孔中,通过荧光分选(右图;改编自 Lab Chip (2014) 14, 402‑414 经英国皇家化学学会批准。) 数据提供: O. Guilaume-Gentil, 瑞士苏黎世联邦理工学院。
创新与直观地操作
凭借其触摸屏界面和预定义的实验工作流程,例如单细胞注射和提取或细菌和细胞粘附力测量,直观的FluidFM ARYA操作员软件将指导您逐步完成每个实验。
所有的FluidFM探针都采用无菌泡壳包装并预安装在塑料载片夹上.每个泡壳包装外面都有一个二维码,通过Flex-FPM系统配置的二维码读码器能够读取,以便将详细的悬臂信息直接导入操作员软件中。
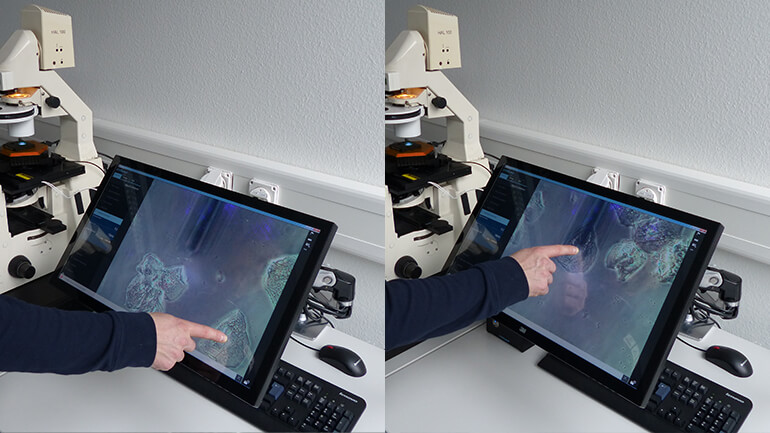

Flex-FPM 应用示例
细胞-细胞间粘附力
最近,FluidFM™细胞黏附力测量被扩展到研究细胞与细胞之间的相互作用。这可以是一个细胞(在悬臂梁上)和位于基底上的细胞(图1A)之间的力,也可以是细胞和它周围位于融合层中的细胞(图1B)之间的力。
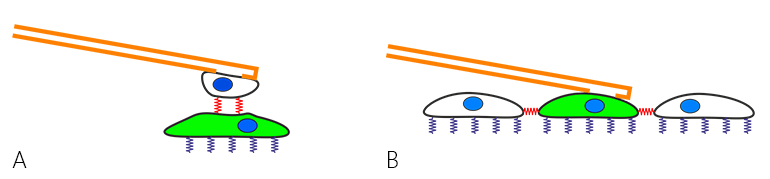
图1:通过将单细胞吸入空心FluidFM™探针(橙色)研究细胞 - 细胞相互作用(红色弹簧)。A)探测固定在悬臂上的细胞和基质上的细胞之间的力,B)从融合层中挑选单个细胞,探测细胞 - 基质(紫色)和细胞 - 细胞(红色)相互作用。
波士顿东北大学Tanya Konry教授小组的Noa Cohen博士用Flex-FPM系统研究细胞间粘附力,以更深入地了解肿瘤的进展和转移情况[Cohen et al. (2017)].图2示出了Cohen在本研究中使用方法的光学图像。

将单个MCF7乳腺癌细胞固定在悬臂上。然后将细胞推到固定在基质上的不同细胞类型上。发现MCF7癌细胞与不同细胞类型之间测量的细胞粘附力随着培养时间而有不同的发展。在这些实验中,细胞的可逆结合使得可以用相同的探针来测不同的细胞间力(图3),从而更好地比较测量值。
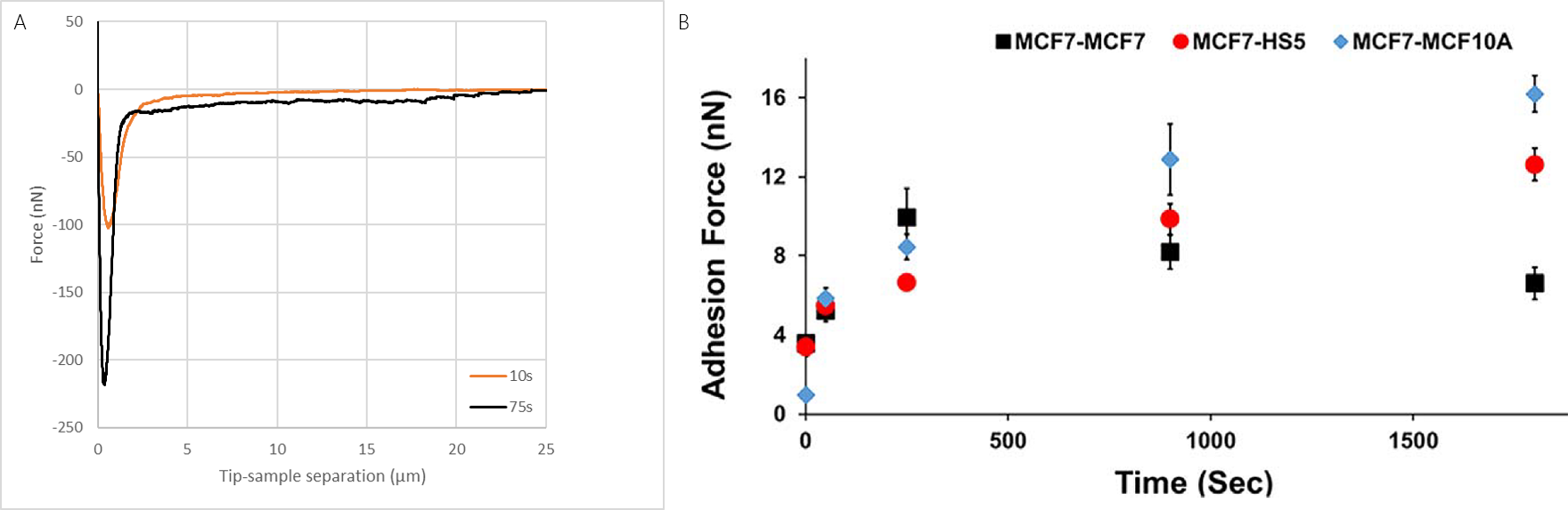
图3A)不同接触时间探针上MCF7细胞与基底上非癌变成纤维细胞(HS5)之间的典型受力曲线。B)随着接触时间的细胞间粘附力的发展。数据由美国波士顿东北大学Tanya Konry group提供。
来自维尔茨堡大学JürgenGroll教授小组的Ana Sancho博士广泛研究了上皮细胞融合层中细胞与其相邻细胞之间的相互作用(图2B)[Sancho et al. (2017)]。图4显示悬臂从融合层(A)拾取细胞。移除后,可以看到拾取细胞的空白区域(B)。同样,可以使用倒置显微镜基于细胞大小和细胞形状来选择感兴趣的上皮细胞。
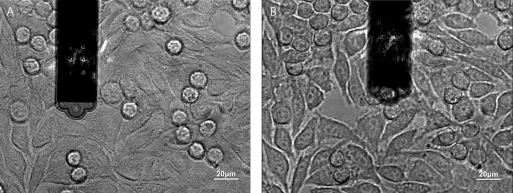
图4:融合层细胞,其中一个被FluidFM拉出,改编自:Sancho等人(2017),《科学报告》第7卷46152页。
我们发现来自脐动脉的人类内皮细胞具有强大的细胞间力(图6A和B)。通过过量所谓的 (MSX1)蛋白可以显著降低这种细胞间力。MSX1诱导内皮细胞向间质转化。这种转变涉及心血管发育和发病的过程。除了这些粘附实验之外,Flex-FPM系统还被用于纳米压痕测量。为此,悬臂拾取胶体珠并记录在细胞上的力曲线。
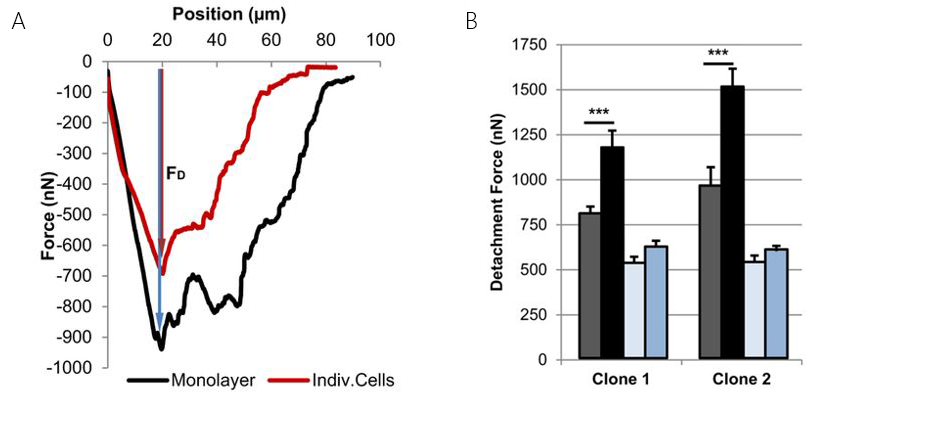
图5:A)单个细胞间或融合层细胞间的典型单细胞力曲线,描绘了细胞-细胞相互作用引起粘附力的增加。B)MSX1对那些单个细胞间和单层细胞之间黏附的影响效果。灰色和黑色条:分别对单个细胞间和单层细胞间进行的对照测量,浅色和浅蓝色条:分别对MSX1处理过的单个细胞间和单层细胞间进行的测量。来源:Sancho等(2017年),科学报告第7卷,46152。/div>
这两个例子都大大得益于Flex-FPM提供的FluidFM™技术。在融合层的情况下,高达1.5μN以上的粘附力消除了化学绑定力以研究细胞间粘附力。在这两例情况下,可逆的结合为实验提供了必要的省时以获得足够的统计数据。
使用FluidFM进行点识别和光刻
在细胞生物学中,微图案研究正成为一种广泛接受的技术,用于锁定单细胞水平的细胞行为。例如,可以通过局部抑制或刺激来引导细胞生长,这极大地有利于研究细胞生长,开发基于细胞的传感器和组织工程应用。微制造生物传感器的生产是另一种需要将生物材料精确放置在基体上的应用。
Cytosurge的FluidFM®技术可以将(生物)分子和颗粒沉积在具有微米精度和飞秒体积的特定位置。封闭通道能够在空气和液体环境中从液体中沉积分子。这使得生物医学,细胞和微生物学以及非生物纳米光刻技术中的许多应用成为可能。

在网格状图案(每种条件3个点)自动地变更背压和接触时间,点的尺寸可以迅速优化。

用含有约50%甘油的溶液在空气中写的Nanosurf商标; 背压200毫巴。





